کلمه conversion در زبان انگلیسی به معنی تبدیلات یک طرفه و غیر قابل برگشت است. این کلمه برای بیان تبدیل فاز های سیلیس به کار می رود. دلیل استفاده از این کلمه برای بیان تبدیلات فاز های سیلیس تقریبا مشخص است. به طور خلاصه این کلمه به این دلیل در این مورد استفاده می شود که تبدیل فاز های سیلیس بسیار کند بوده و در شرایط معمولی به سادگی قابل برگشت نیستند و بنابراین در هنگام برگشت، فاز های پایداری را به وجود نمی آورند.
به عنوان مثال فاز های کریستوبالیت و یا تریدیمیت تحت فشار سرد شوند، مانند نمودار تعادلی سیلیس عمل نموده و فاز تریدیمیت به کوارتز و فاز کریستوبالیت ابتدا به تریدیمیت و سپس به کوارتز تبدیل می شوند. به همین دلیل نیز در طبیعت سیلیس معمولا به شکل کواتز یافت شده و به ندرت فاز های تریدیمیت و کریستوبالیت را می توان به طور طبیعی یافت، چرا که این فاز ها در طبیعت تحت فشار سرد می شوند.
نباید تصور کرد که فاز های نیمه پایدار سیلیس فقط در هنگام سرد شدن به وجود می آیند. در هنگام گرم شدن، چنانچه زمان لازم برای تبدیلات به آن ها داده نشود باز هم فاز های نیمه پایدار ایجاد می شوند. به عنوان مثال هنگامی که کوارتز سریعا گرم شود این فاز در درجه حرارتی بسیار کم تر از آن چیزی که منحنی تعادلی نشان می دهد یعنی در حرارتی حدود 1460 ذوب می شود.
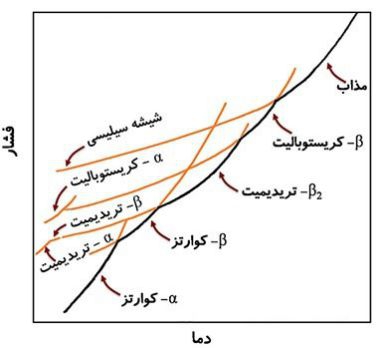
تحولات فاز ی سیلیس
کوارتز، تریدیمیت، کریستوبالیت و سیلیس مایع چهار فاز پایدار سیلیس در شرایط تعادل هستند. کوارتز فاز پایدار در شرایط معمولی محیط است. فاز کوارتز تا درجه حرارت 870 درجه سانتی گراد هم چنان به صورت پایدار باقی مانده و سپس طبق منحنی تعادلی به تریدیمیت تبدیل می شود. تریدیمیت نیز به صورت پایدار بین درجه حرارت های 870 تا 1470 درجه سانتی گراد وجود داشته و پس از آن کریستوبالیت در درجه حرارت 1470 به وجود می آید و در نهایت کریستوبالیت در 1713 درجه سانتی گراد ذوب شده و فاز سیلیس مایع ایجاد می شود. تبدیلات مذکور در عمل و به خصوص در مقیاس تولید صنعتی به همان سادگی که دیاگرام فازی نشان می دهد به وقوع نمی پیوندد. تبدیل فاز های سیلیس در عمل بسیار به کندی صورت پذیرفته و اغلب مدت زمان بسیار زیادی را لازم دارند تا به تعادل برسند. زیرا این عمل مستلزم شکسته شدن پیوند چهار وجهی ها و اتصال مجدد آن ها به شکل جدید است. به عنوان مثال تبدیل کوارتز به تریدیمیت آنقدر آرام و کند است که عملا بدون استفاده از کاتالیزور ها امکان پذیر نیست.برای ایجاد فاز تریدیمیت، ابتدا باید کوارتز تا درجه حرارت تشکیل کریستوبالیت یعنی بالاتر از 1470 و پایین تر از 1713 درجه سانتی گراد سرد شود تا فاز تریدیمیت ایجاد شود. به همین دلیل در فرآورده های سرامیک فاز تریدیمیت کمیاب بوده و معمولا به اندازه فاز های کوارتز، کریستوبالیت و سیلیس مذاب مورد توجه نیست. در بین محصولات سرامیک فاز تریدیمیت در بعضی از آجر های نسوز به طور عمده وجود دارد. در هنگام سرد شدن، تبدیل فازها باز هم مشکل تر شده و به طور عملی در مقیاس صنعتی تقریبا امکان ناپذیر است. در این شرایط عملا فاز های سیلیس مطابق منحنی تعادلی رفتار نکرده و در حالت غیر تعادلی فاز های نیمه پایدار یا metastable ظاهر می شوند.
شکل زیر ضمن مشخص کردن فازهای پایدار سیلیس، فازهای نیمه پایدار را نیز نشان می دهد. در این سیستم پایدارترین فاز ها در یک درجه حرارت مشخص، فازهایی هستند که دارای پایین ترین فشار بخار هستند. این فازهای پایدار در شکل 27 با خطوط سیاه نشان داده شده و فازهای نیمه پایدار که دارای پایین ترین فشار بخار نیستند با خطوط نارنجی مشخص شده اند. همچنان که در این شکل مشخص است عملا در هنگام سرد شدن، فاز سیلیس مایع به کریستوبالیت تبدیل نشده بلکه شیشه سیلیسی را به وجود می آورد، به همین ترتیب هنگامی که فاز پایدار کریستوبالیت β تا درجه حرارتی کمتر از 1470 درجه سانتی گراد سرد می شود به تریدیمیت تبدیل نشده و در درجه حرارت اتاق فاز نیمه پایدار کریستوبالیت α وجود خواهد داشت. تریدیمیت نیز حین سرد شدن رفتاری مشابه کریستوبالیت را نشان می دهد، در هنگام سرد شدن، تریدیمیت β2 به فاز کوارتز تبدیل تبدیل نشده بلکه ابتدا فاز نیمه پایدار تریدیمیت β و سپس فاز نیمه پایدار تریدیمیت را در درجه حرارت اتاق به وجود می آورد.
طراحان تصفیه






Copyright © 2019 کلیه حقوق مادي و معنوي این سایت محفوظ و متعلق به شرکت طراحان تصفیه مي باشد . هرگونه کپی برداری با ذکر منبع بلا مانع است
لینکهای ارتباطی شرکت
ایمیل
co_ttk@yahoo.com
تلگرام
Telegram ID : @ttkco
کانال
Telegram channel : @ttkwater
اسکایپ
Skype: ttkwater
تلفن
02636107120
02636107130
02636107251
02636107248
02636107950
فکس
02636107949
آدرس شرکت:
جاده مخصوص تهران-کرج
کیلومتر 26
خیابان سروستان
کوچه سوم غربی
پلاک 165

